Was ist derOberflächenspannung von Wasser?
Oberflächenspannungist die Tendenz von Flüssigkeitsoberflächen, sich auf die kleinstmögliche Oberfläche zu verkleinern. Die Oberflächenspannung ermöglicht es Objekten mit einer höheren Dichte als Wasser, wie Rasierklingen und Insekten (z. B. Wasserläufern), auf einer Wasseroberfläche zu schwimmen, ohne auch nur teilweise unterzutauchen.
An Flüssigkeits-Luft-Grenzflächen entsteht die Oberflächenspannung durch die stärkere Anziehung der Flüssigkeitsmoleküle zueinander (aufgrund Kohäsion) als zu den Molekülen in der Luft (aufgrund Adhäsion).
Dabei spielen zwei Hauptmechanismen eine Rolle. Einer ist eine nach innen gerichtete Kraft auf die Oberflächenmoleküle, die dazu führt, dass sich die Flüssigkeit zusammenzieht. Der zweite ist eine tangentiale Kraft parallel zur Oberfläche der Flüssigkeit. DiesetangentialKraft wird im Allgemeinen als Oberflächenspannung bezeichnet. Der Nettoeffekt ist, dass sich die Flüssigkeit so verhält, als ob ihre Oberfläche mit einer gespannten elastischen Membran bedeckt wäre. Diese Analogie darf jedoch nicht zu weit getrieben werden, da die Spannung in einer elastischen Membran vom Ausmaß der Verformung der Membran abhängt, während die Oberflächenspannung eine inhärente Eigenschaft der Flüssigkeit ist.–Luft oderFlüssigkeit-DampfSchnittstelle.
Aufgrund der relativ hohen Anziehungskraft der Wassermoleküle untereinander durch ein Netz von Wasserstoffbrücken hat Wasser eine höhere Oberflächenspannung (72,8 Millinewton (mN) pro Meter bei 20 Grad) als die meisten anderen Flüssigkeiten. Die Oberflächenspannung ist ein wichtiger Faktor beim Phänomen der Kapillarität.
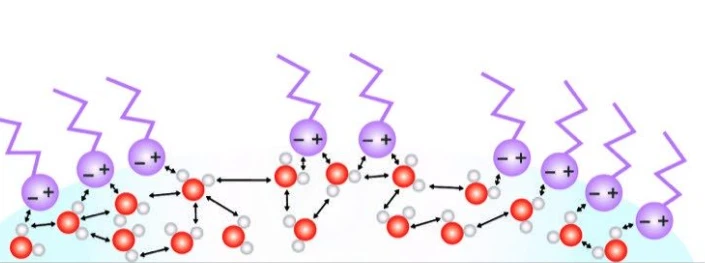
Warum zerstört Seife die Oberflächenspannung von Wasser?
Seife unterbricht die Oberflächenspannung von Wasser aufgrund ihrer Molekülstruktur, die sowohl hydrophobe (wasserabweisende) als auch hydrophile (wasseranziehende) Enden enthält. Wassermoleküle an der Oberfläche bilden aufgrund der Kohäsionskräfte zwischen ihnen eine „Haut“, was zu einer hohen Oberflächenspannung führt.
Wenn Seife dem Wasser zugesetzt wird, werden die hydrophoben Enden der Seifenmoleküle vom Wasser abgestoßen und drängen sich an die Oberfläche, während die hydrophilen Enden im Wasser verbleiben. Dadurch werden die Kohäsionskräfte zwischen den Wassermolekülen an der Oberfläche gestört und die Oberflächenspannung verringert. Dadurch wird die Kohäsionskraft des Wassers verringert und es verteilt sich leichter, wodurch es Oberflächen besser benetzen kann.





